
研究成果(图源: Molecular Cancer)
2022年1月4日,来自香港中文大学医学院、中山大学附属第七医院的研究团队在Molecular Cancer在线发表了题为“CircRTN4promotes pancreatic cancer progression through a novel CircRNA-miRNA-lncRNApathway and stabilizing epithelial-mesenchymal transition protein”的文章。研究人员在胰岛管腺癌(PDAC)中发现了一个新的促癌的circRNA- miRNA – lncRNA信号通路,且这3个分子均是非编码RNA。除了调节lncRNA的表达外,研究还发现circRTN4能与上皮间质转化(epithelial-mesenchymaltransition, EMT)驱动蛋白RAB11FIP1相互作用,增强其稳定性并促进EMT发生。研究结果拓宽了对circRNA在PDAC基因表达调控中的作用的认识。
在前期工作的基础上,研究人员重点关注一种名为circRTN4的环状RNA。细胞水平的检测显示,circRTN4在几种不同类型的PDAC细胞系中均显著上调。在88例PDAC患者中,circRTN4上调的患者比例高达60%。此外,在结直肠癌、喉部鳞状细胞癌、头颈部鳞状细胞癌、卵巢癌、肾癌等多种肿瘤中也出现类似的结果。研究团队分析了circRTN4的表达水平与临床特征之间的相关性,发现肝转移的PDAC患者原发肿瘤中circRTN4表达水平显著上调,提示PDAC原发肿瘤中circRTN4表达上调可能参与了肿瘤肝转移。
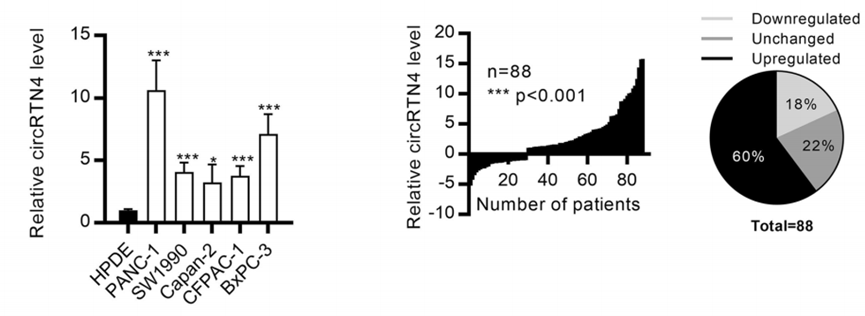
circRTN4在PDAC细胞和原发性肿瘤中上调(图源: Molecular Cancer)
为验证这种相关性是否具有因果关联,研究人员进行了细胞水平的circRNA敲降实验,发现敲降circRNA后,PDAC细胞系的增殖、克隆形成、迁移和侵袭能力均较对照组明显减弱。
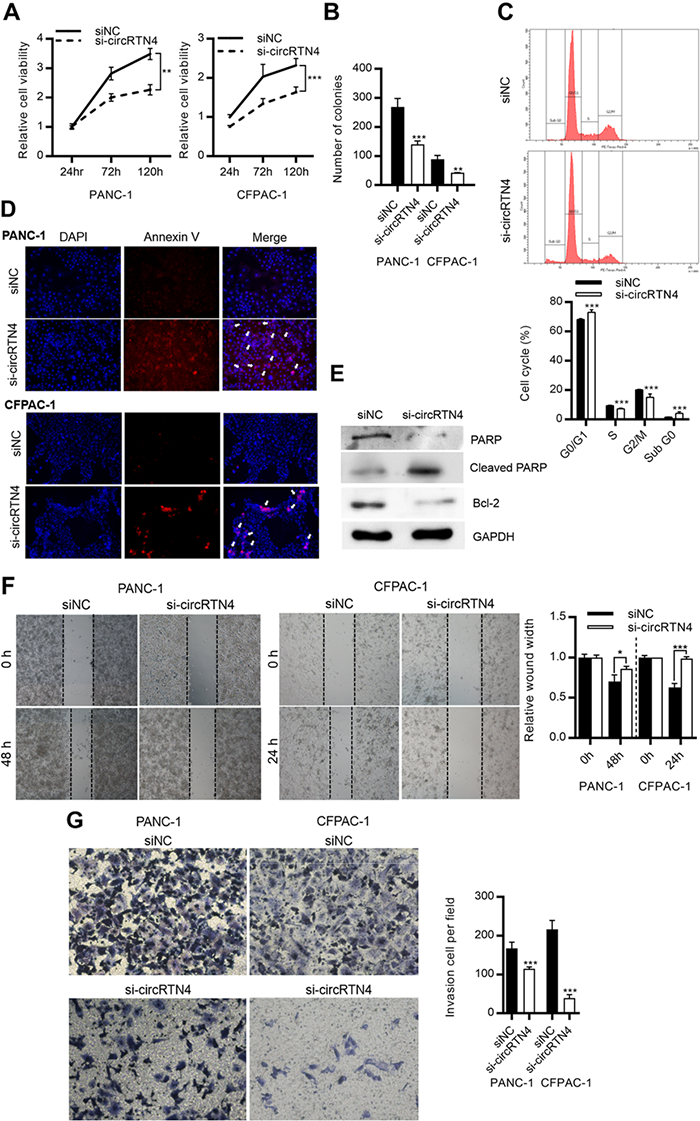
circRTN4促进PDAC细胞的生长、迁移和侵袭(图源: Molecular Cancer)基于小鼠移植瘤模型体内实验进一步证实了抑制circRNA后,肿瘤的生长放缓,凋亡增加,肝转移减少。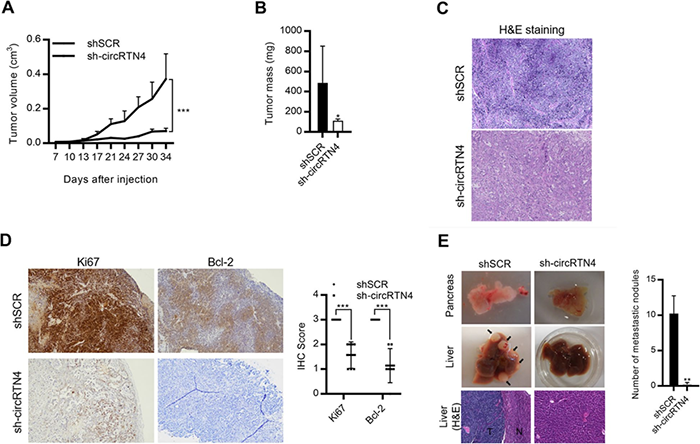
circRTN4促进PDAC肿瘤生长和肝转移(图源: Molecular Cancer)体内、体外实验结果充分说明了circRTN4在促进PDAC细胞生长和侵袭中的重要性。接下来,研究人员试图寻找该分子发挥作用的具体分子机制。借助生物信息学预测软件,研究人员筛选了可能与circRTN4结合的miRNA,随后通过荧光素酶报告分析、miRNA pull down、生物素标记等多种实验手段证实了PDAC细胞circRTN4与miR-497-5p存在相互作用,并且circRNA通过经典的“sponge”(吸附)效应,抑制miR-497-5p的功能。此前已有多个文献报道miR-497-5p通过靶向致癌HOTTIP-HOXA13通路( HOTTIP是来源于HOXA的5′端的一个长链非编码RNA。HOTTIP-HOXA13与疾病发生的关系非常密切)在PDAC中发挥抑癌作用。那么,circRTN4会否通过“sponge”效应抑制PDAC中的miR-497-5p,从而调控HOTTIP-HOXA13通路?相关的实验数据显示,circRTN4的确通过抑制miR-497-5p,影响了lncRNA HOTTIP的表达,首次在PDAC中发现了由3个不同类型的非编码RNA组成的circRTN4-miR-497-5p-lncRNAHOTTIP这一信号轴。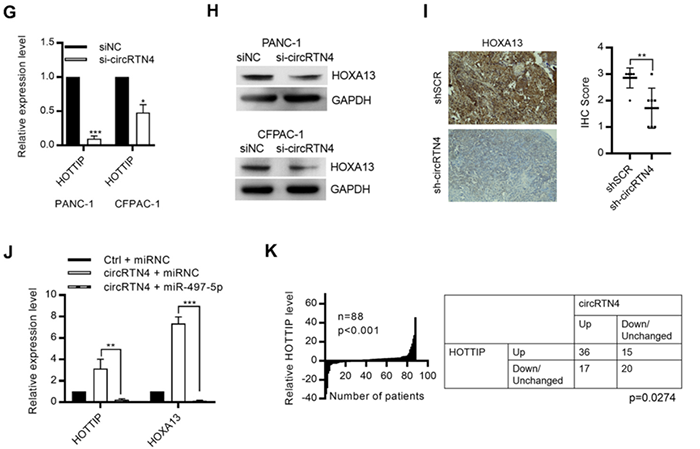
circRTN4通过在PDAC中“吸附”miR-497-5p来促进HOTTIP的表达(图源: Molecular Cancer)尽管circRNA-miRNA这种相互作用模式是circRNA在PDAC中报道最多的模式,但许多细胞系中circRNA的丰度都比miRNA低得多,表明circRNA在PDAC中可能有其他独立于miRNA的作用机制。为解决这个问题,研究人员circRTN4寻找与之相互作用的蛋白质,识别出了EMT驱动因子RAB11FIP1以及其与cirRTN4的结合位点。一系列实验结果显示,cirRTN4通过阻断RAB11FIP1的泛素化来稳定RAB11FIP1,促进N-cadherin、Slug、Snai1、Twist和Zeb1等EMT通路关键分子的表达,最终促进PDAC的EMT。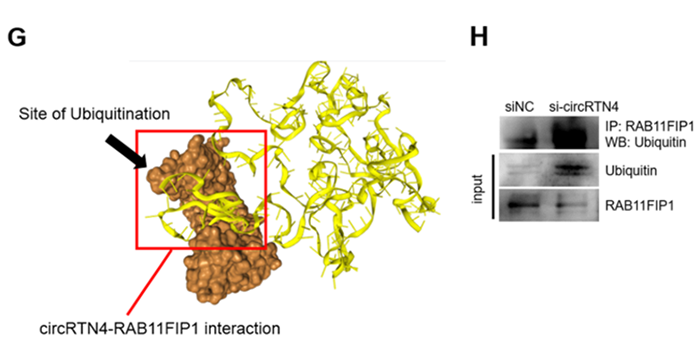
circRTN4通过阻止RAB11FIP1的泛素化和降解来稳定RAB11FIP1(图源: Molecular Cancer)总之,该研究揭示了一种新的促进PDAC进展的circRNA-miRNA-lncRNA途径以及circRTN4通过阻断泛素化促进EMT的机制,为circRTN4的促癌能力提供了新的视角。circRTN4或许能成为一种新的生物标志物和PDAC潜在治疗靶点。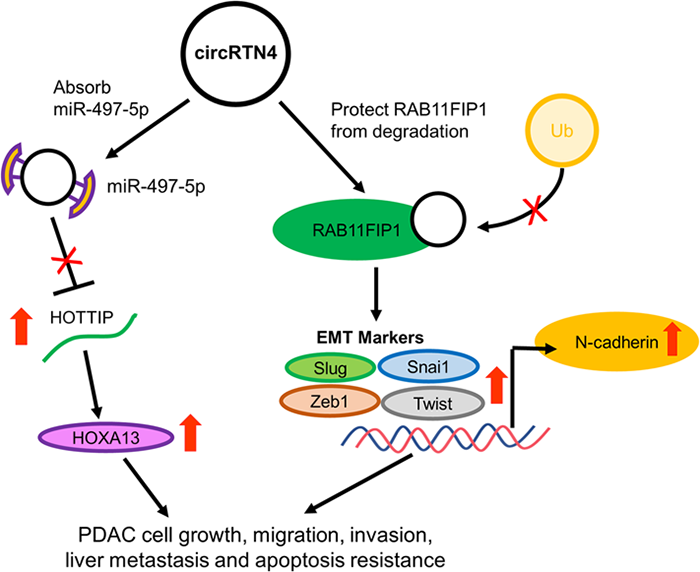
circRTN4促进PDAC发展的机制示意图(图源: Molecular Cancer)[1]Wong CH, Lou UK, Fung FK, et al.CircRTN4 promotes pancreatic cancer progression through a novel CircRNA-miRNA-lncRNA pathway and stabilizing epithelial-mesenchymal transition protein. Mol Cancer. 2022 Jan 4;21(1):10. doi: 10.1186/s12943-021-01481-w. PMID: 34983537.




















